
Текст слайда: Студент − это не сосуд, который надо наполнить, а факел, который надо зажечь Л. Арцимович
Текст слайда: Фенолы
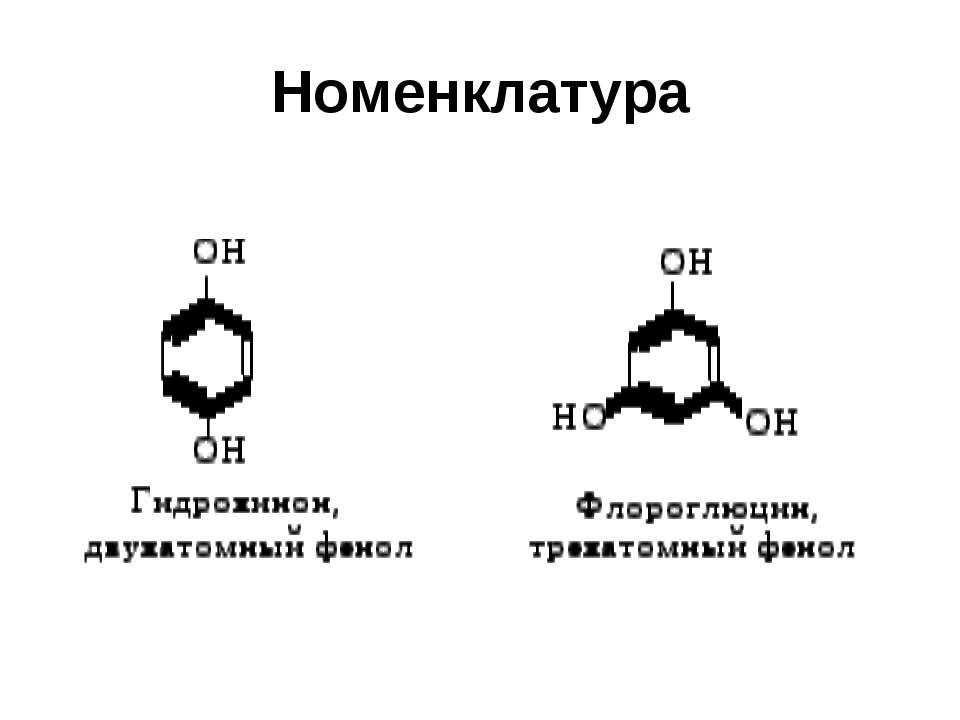
Текст слайда: Номенклатура

Текст слайда: Способы получения фенола Сплавлением натриевой соли бензолсульфокислоты с гидроксидом натрия PhSO3Na + NaOH PhONa + NaHSO3
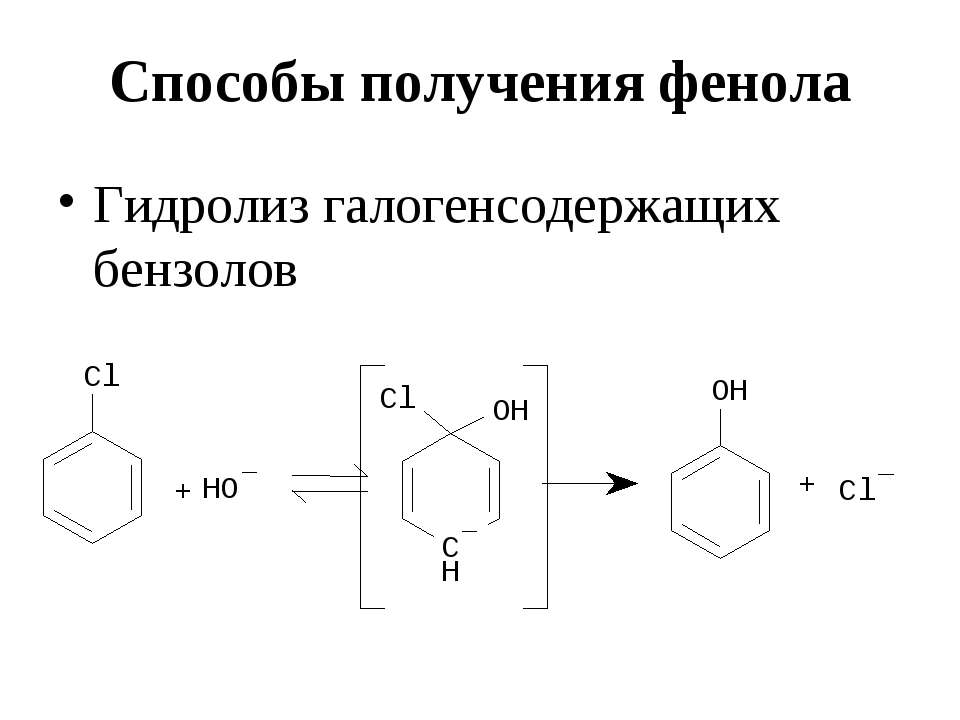
Текст слайда: Способы получения фенола Гидролиз галогенсодержащих бензолов

Текст слайда: Способы получения фенола Из солей диазония [Ph-N+ N]Cl + Н2О PhOH + N2 + НCl Из бензола C6H6 + N2O PhOH + N2
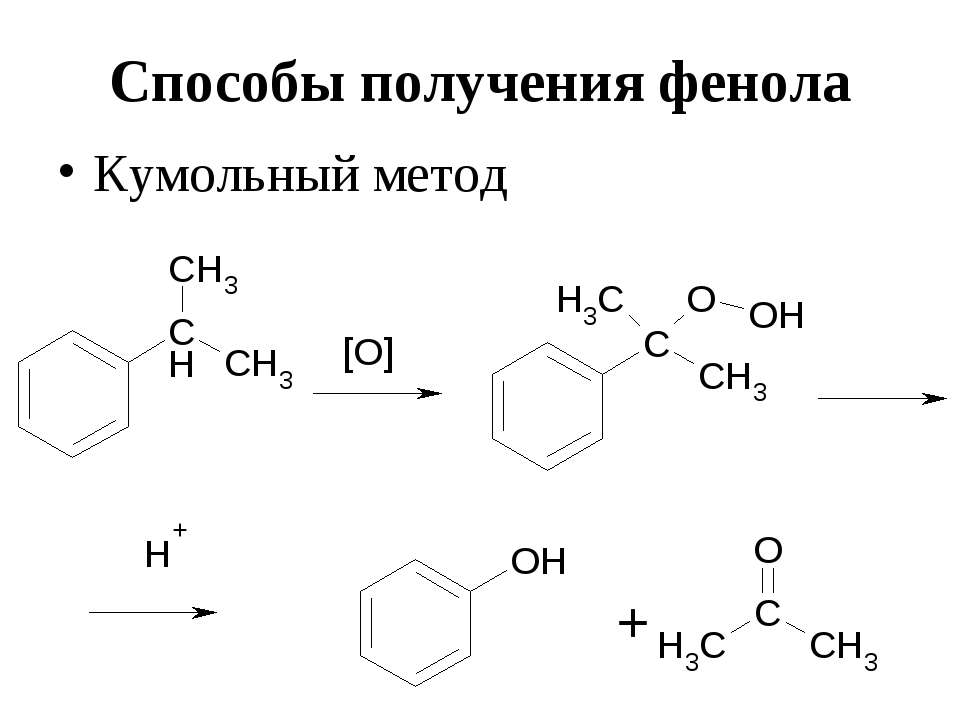
Текст слайда: Способы получения фенола Кумольный метод
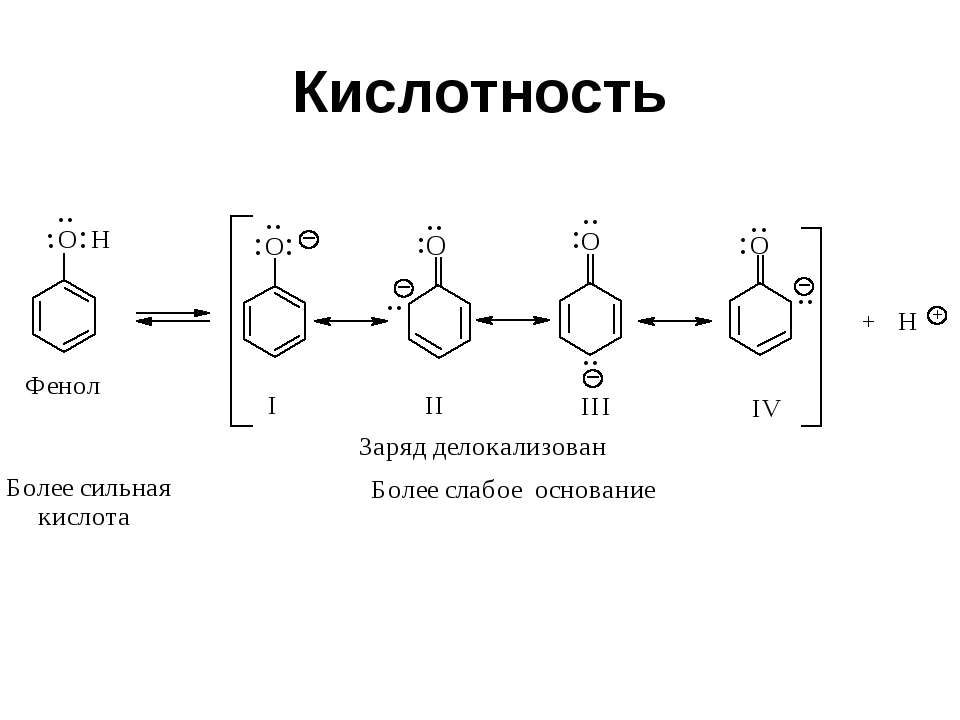
Текст слайда: Кислотность
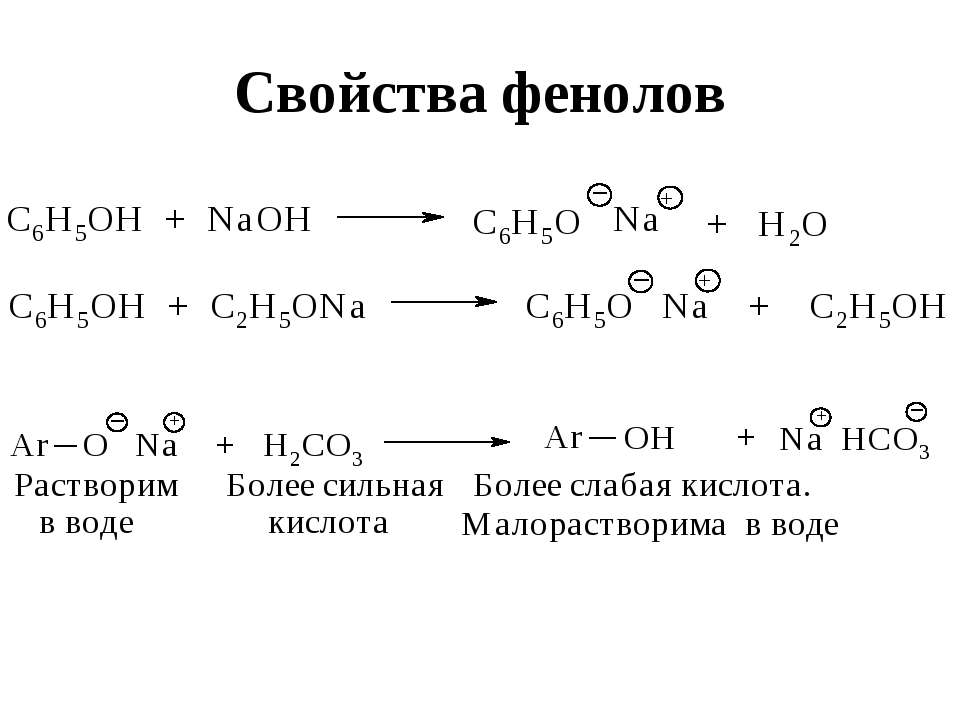
Текст слайда: Свойства фенолов
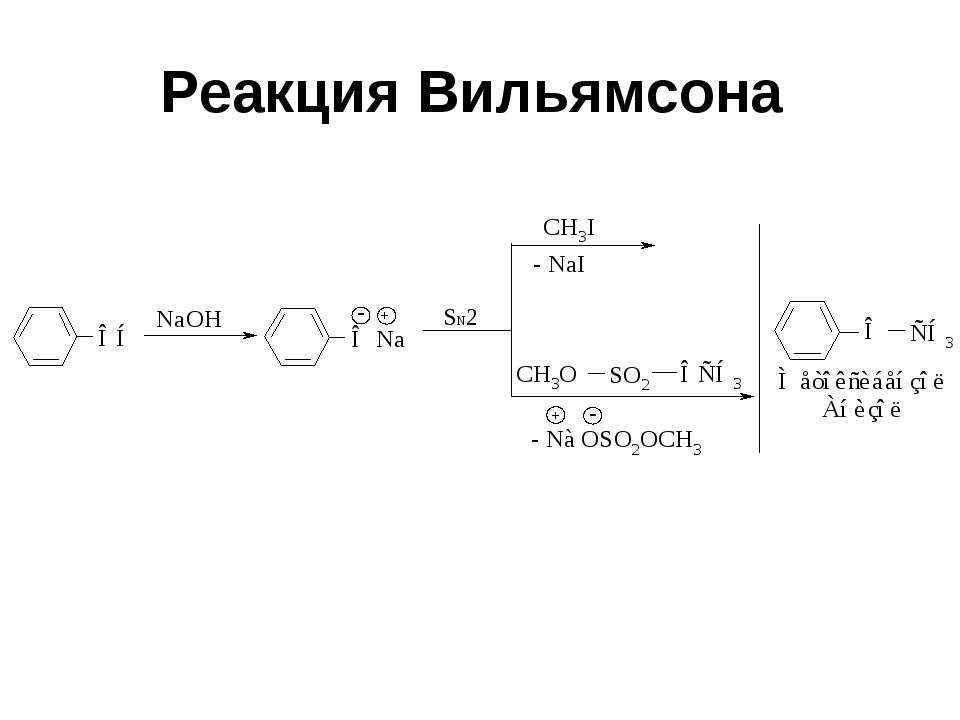
Текст слайда: Реакция Вильямсона
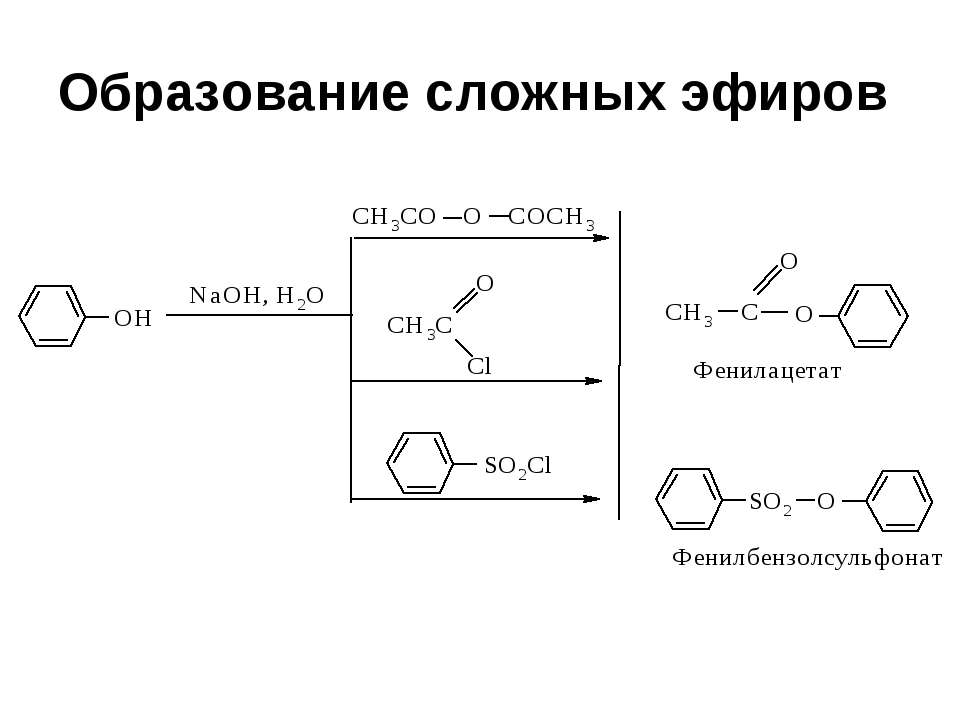
Текст слайда: Образование сложных эфиров

Текст слайда: Свойства фенолов Фенольные соединения взаимодействуют с хлоридом железа (III) и образуют характерные цветные комплексы (качественная реакция)

Текст слайда: Свойства фенолов фенол окрашивает в красно-фиолетовый цвет, крезол - в синий, резорцин - в темно-фиолетовый

Текст слайда: Фенолы Электрофильное замещение в ароматическом ядре
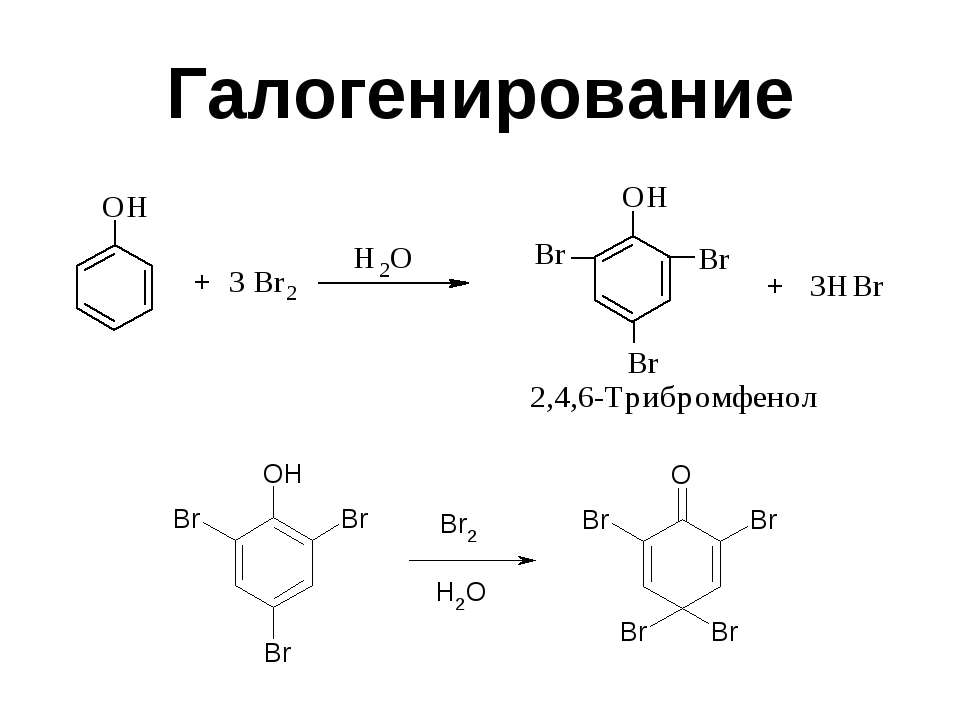
Текст слайда: Галогенирование
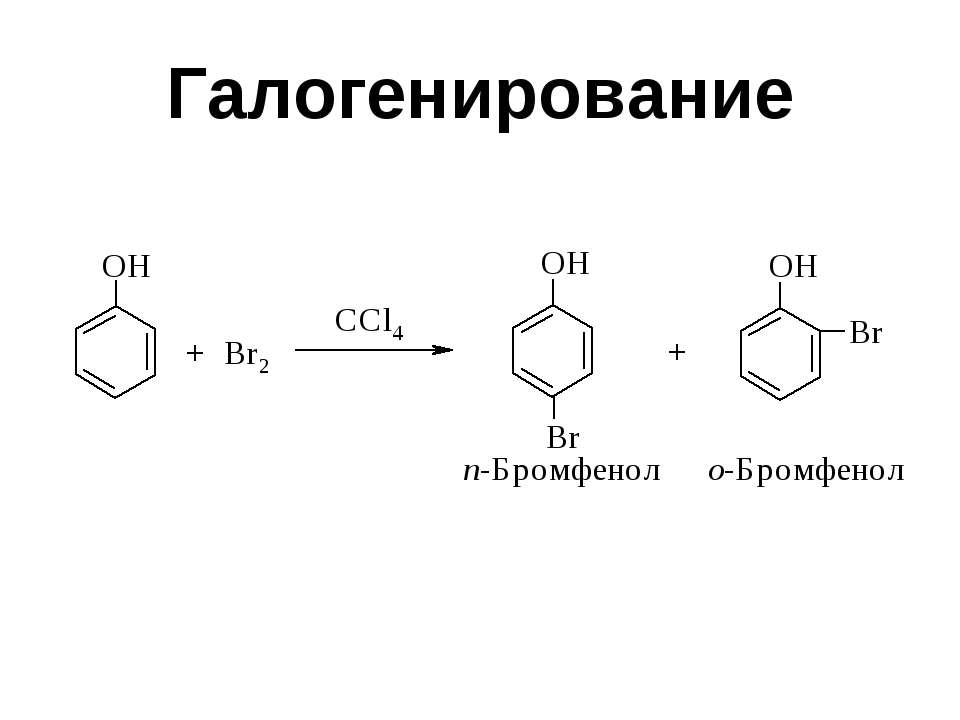
Текст слайда: Галогенирование
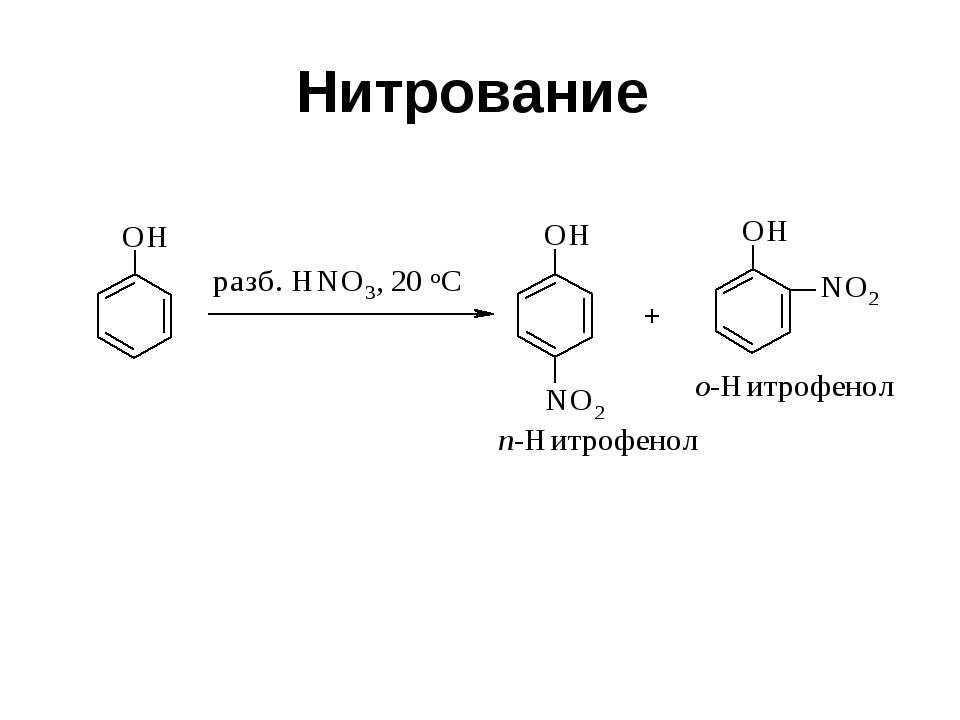
Текст слайда: Нитрование
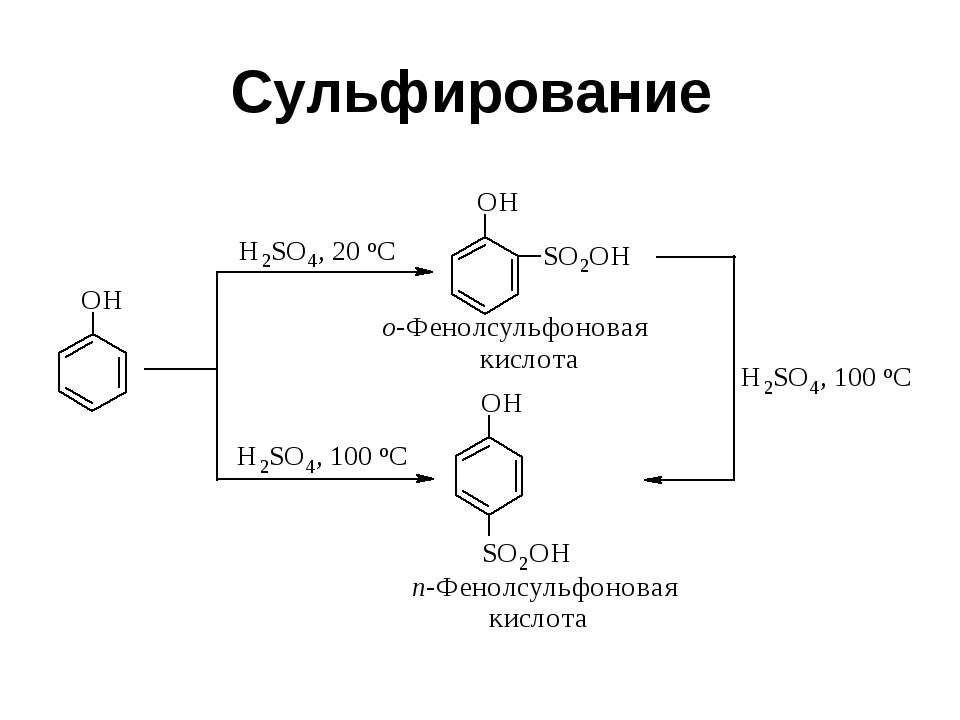
Текст слайда: Сульфирование
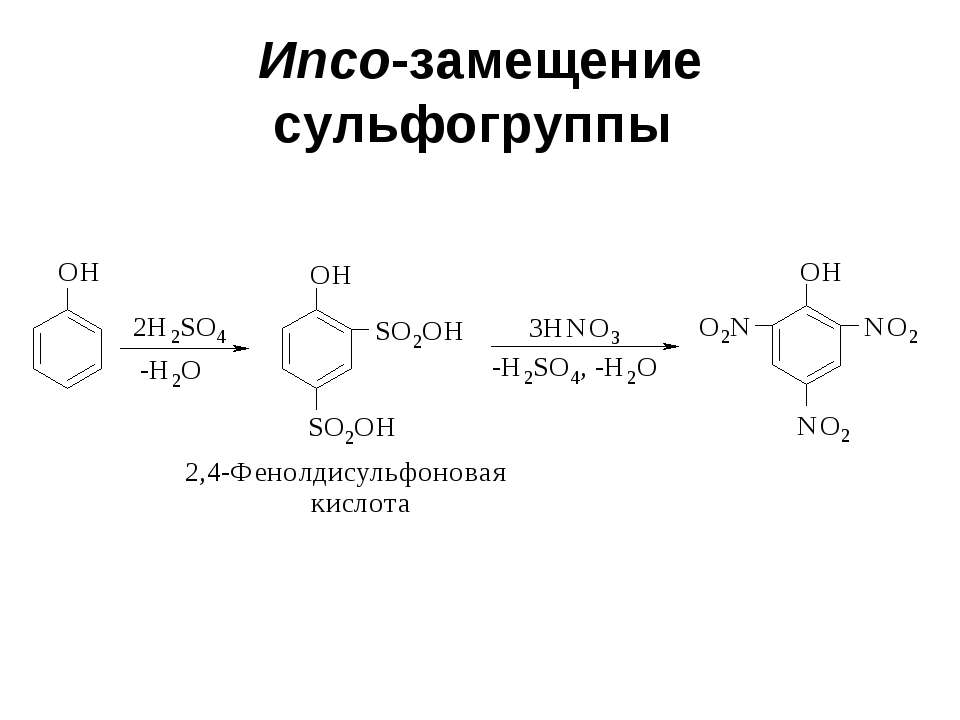
Текст слайда: Ипсо-замещение сульфогруппы
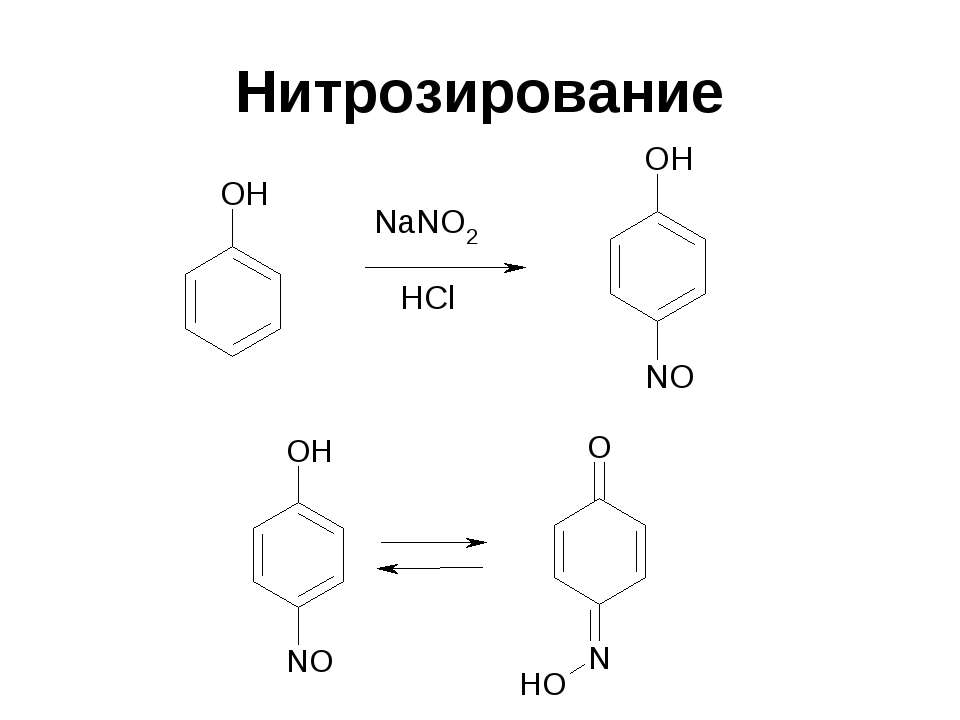
Текст слайда: Нитрозирование
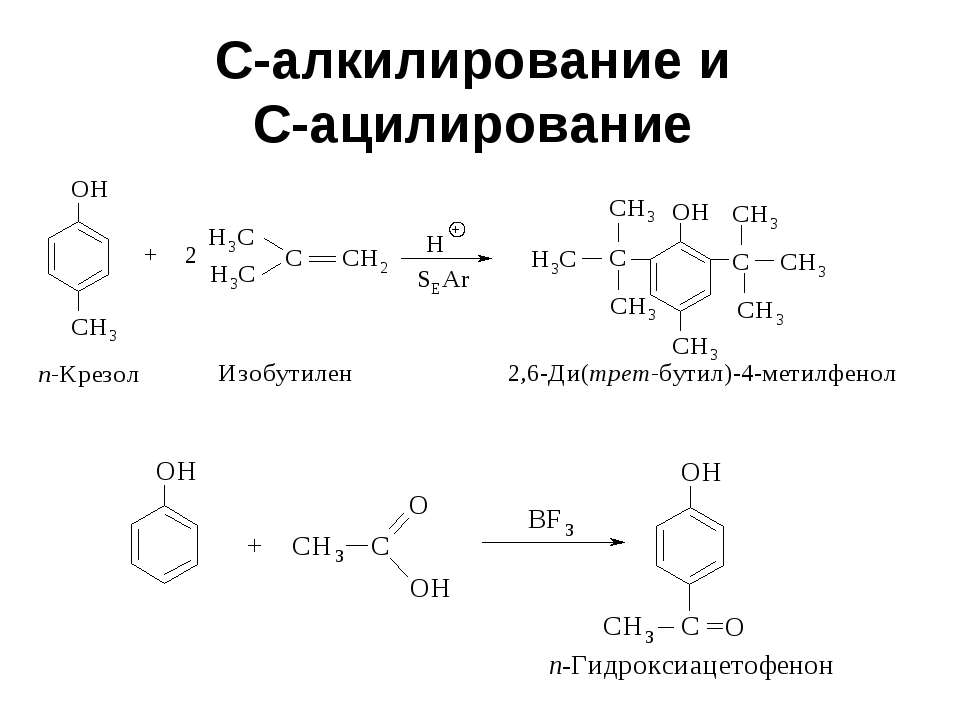
Текст слайда: С-алкилирование и С-ацилирование
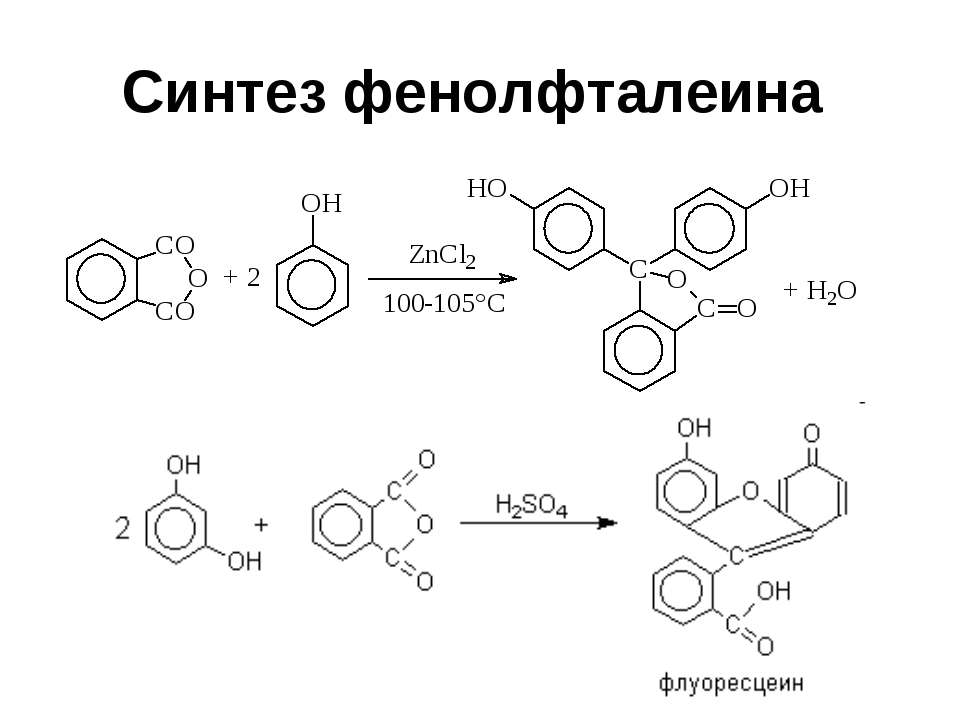
Текст слайда: Синтез фенолфталеина
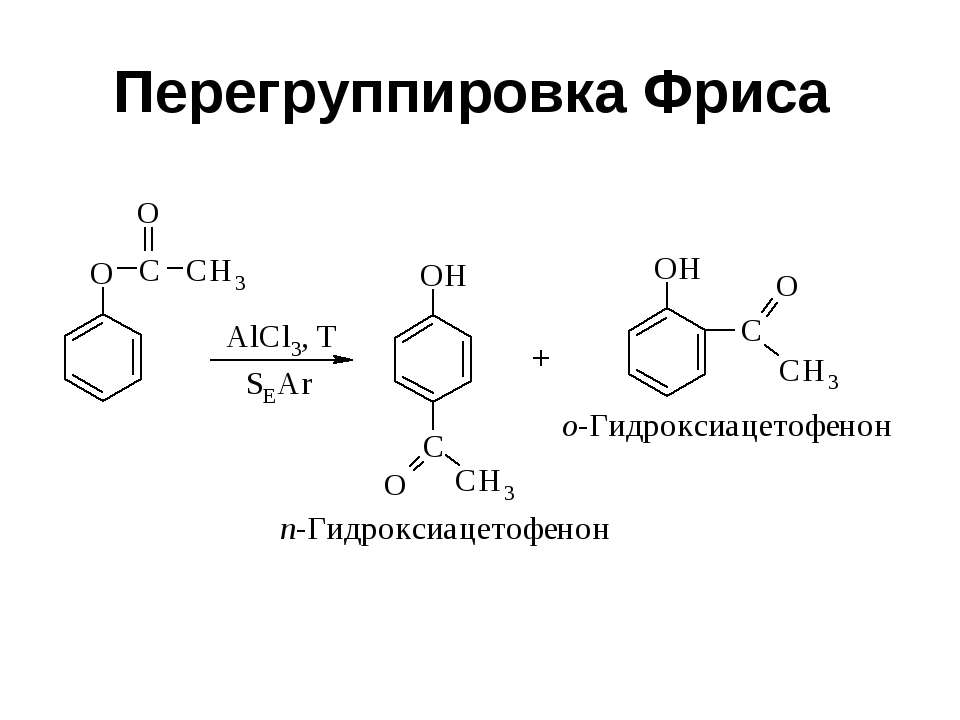
Текст слайда: Перегруппировка Фриса
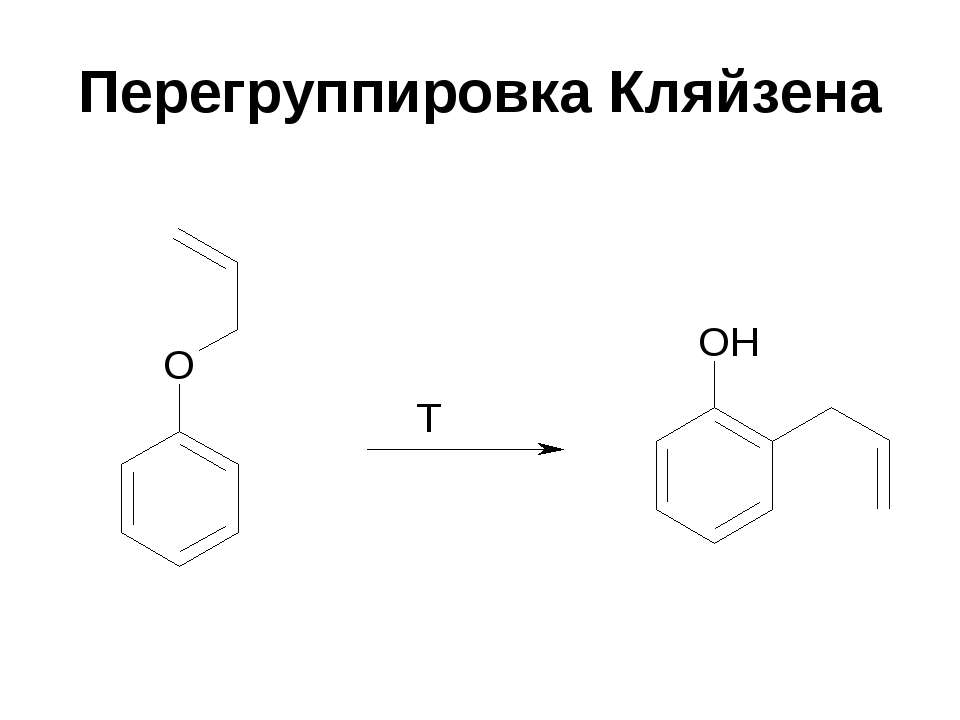
Текст слайда: Перегруппировка Кляйзена
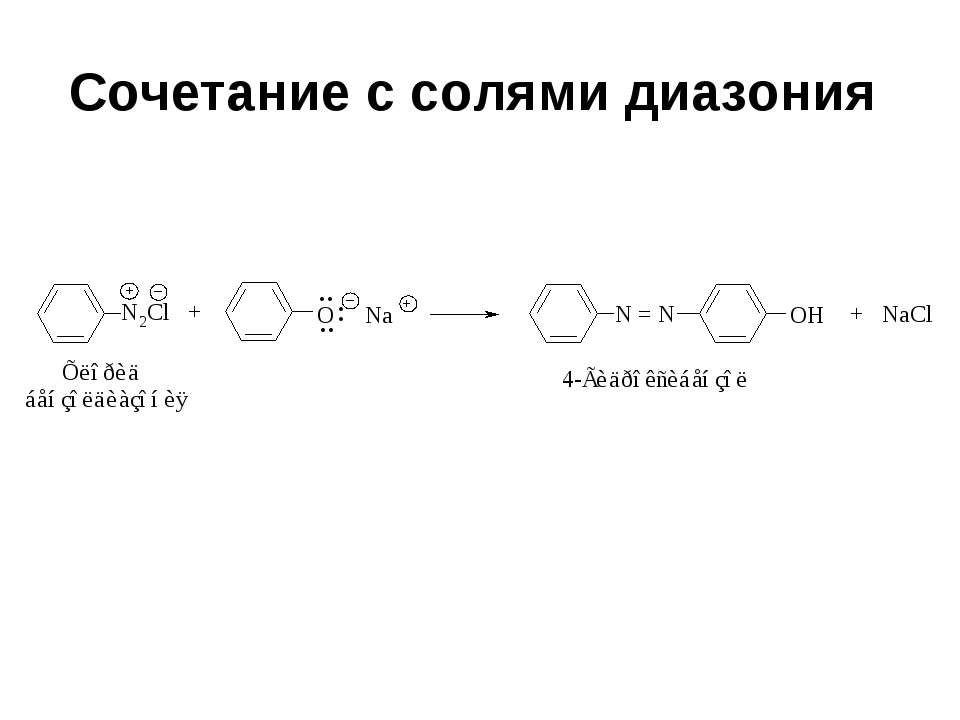
Текст слайда: Сочетание с солями диазония
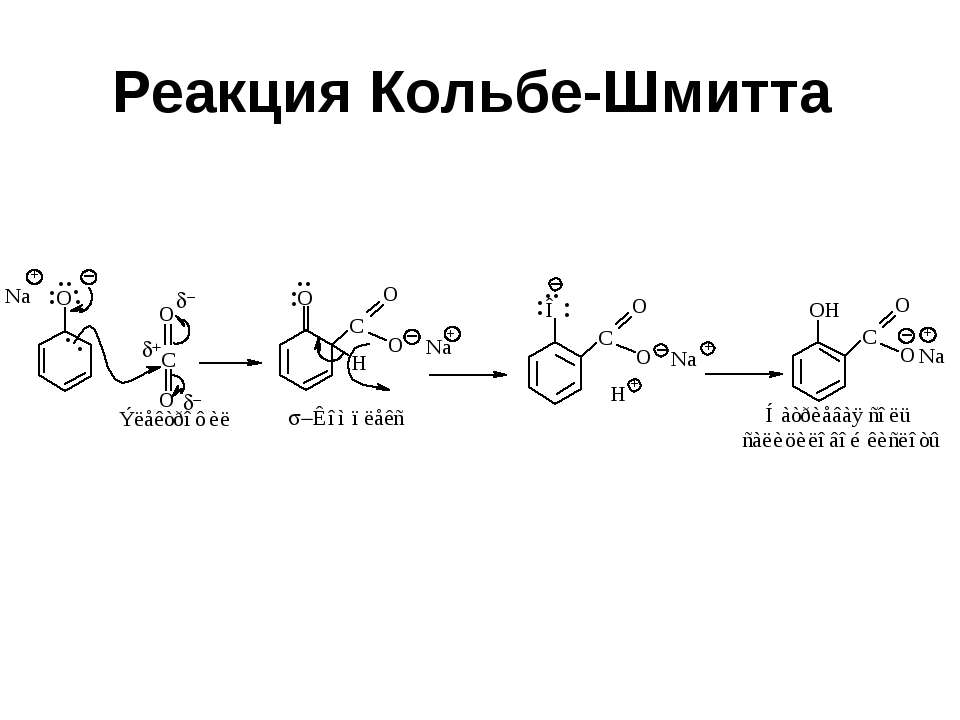
Текст слайда: Реакция Кольбе-Шмитта
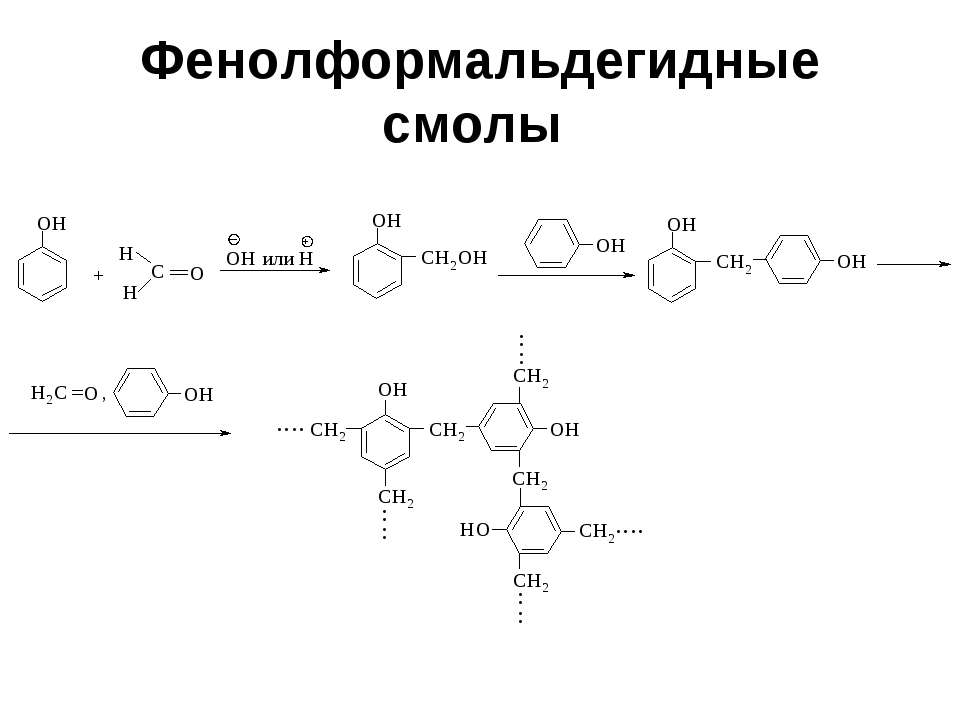
Текст слайда: Фенолформальдегидные смолы
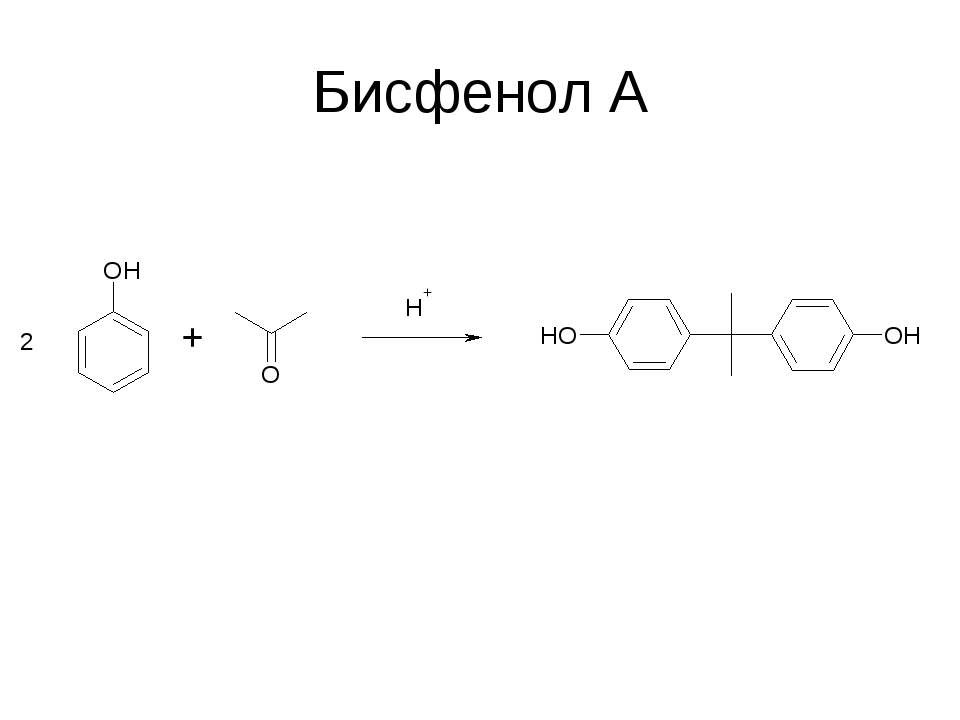
Текст слайда: Бисфенол А
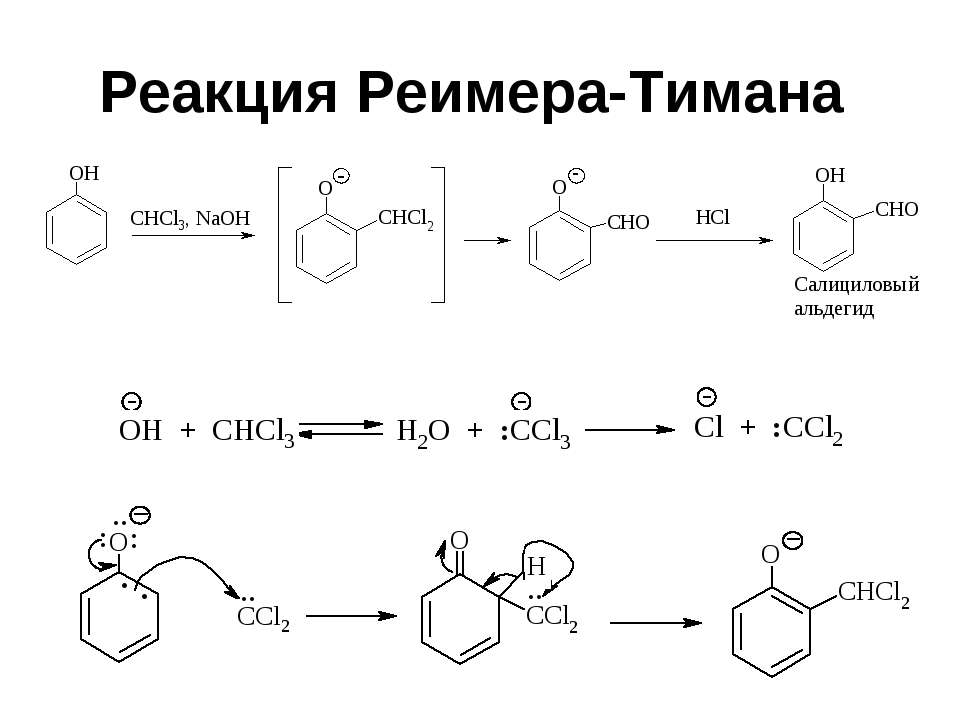
Текст слайда: Реакция Реимера-Тимана
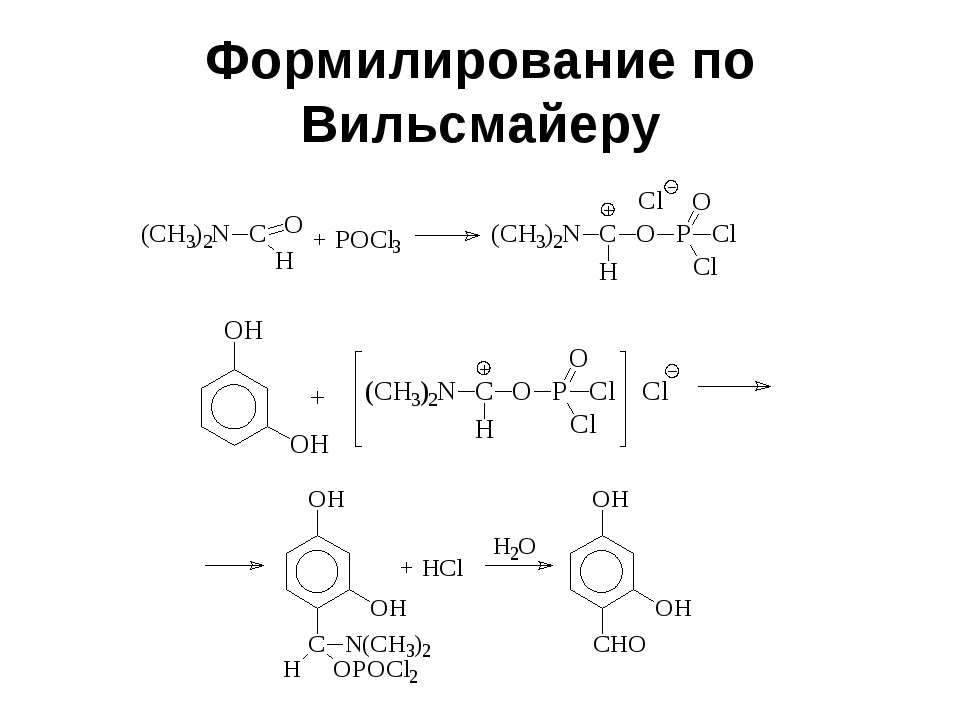
Текст слайда: Формилирование по Вильсмайеру
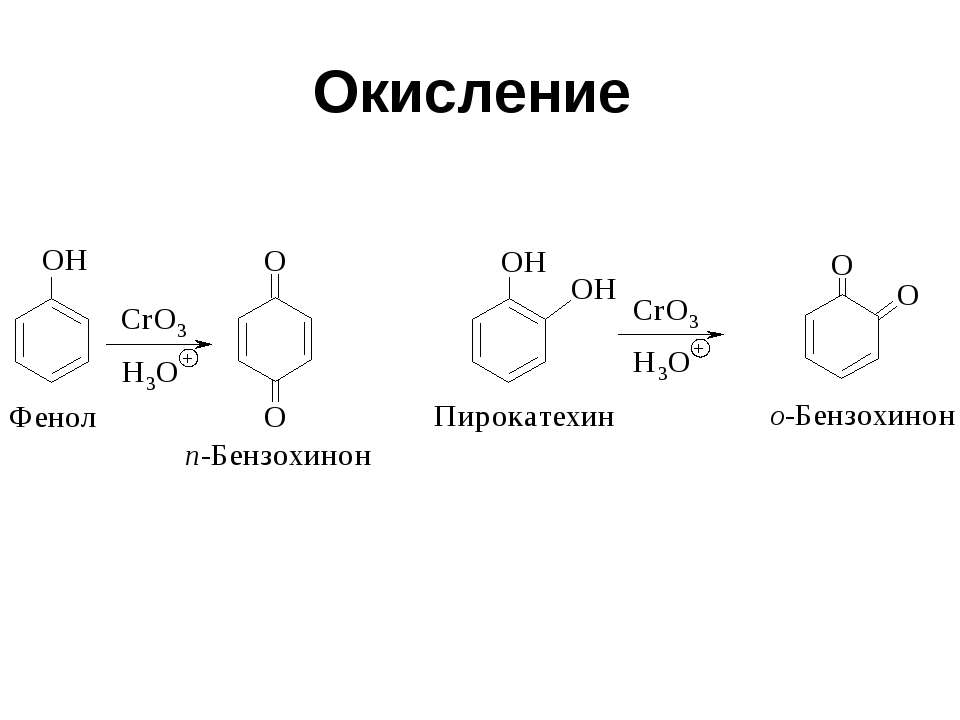
Текст слайда: Окисление

Текст слайда: Окисление Пространственно затрудненных фенолов до феноксильных (ароксильных) радикалов осуществляется под действием гексацианоферрата (III) калия в бинарной системе бензол-вода, диоксида свинца PbO2, оксида серебра или другого одноэлектронного окислителя в индифферентной среде, а также электрохимически
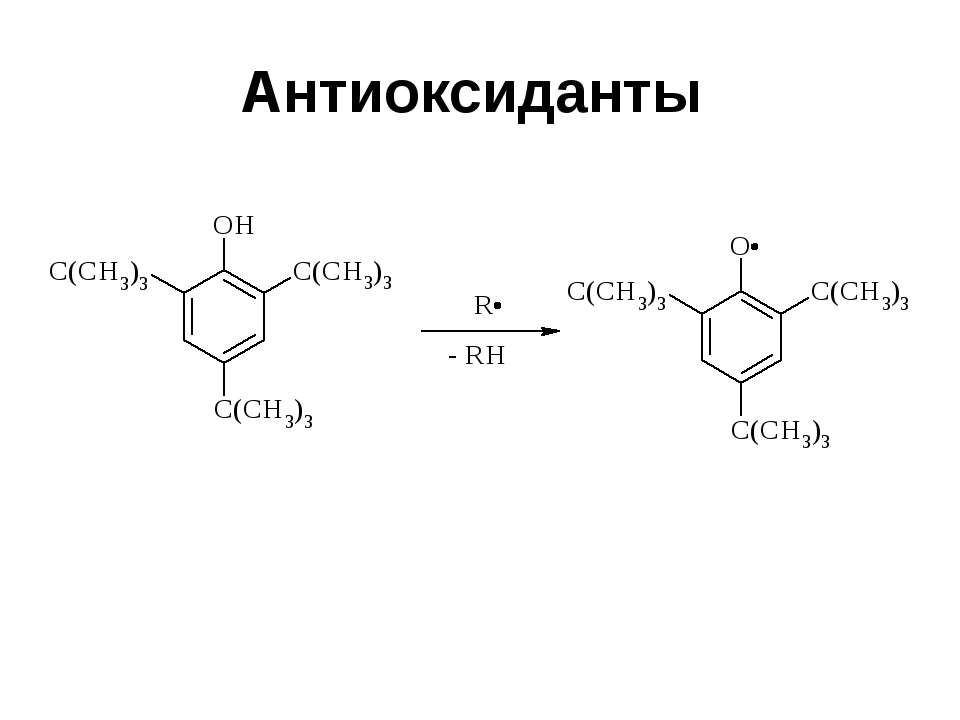
Текст слайда: Антиоксиданты
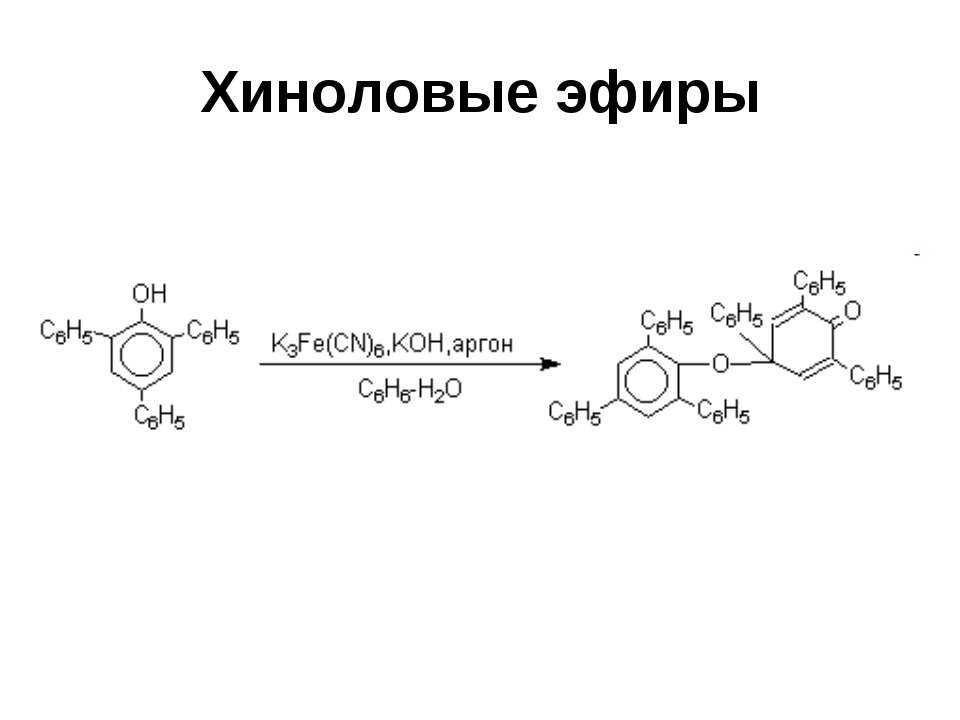
Текст слайда: Хиноловые эфиры
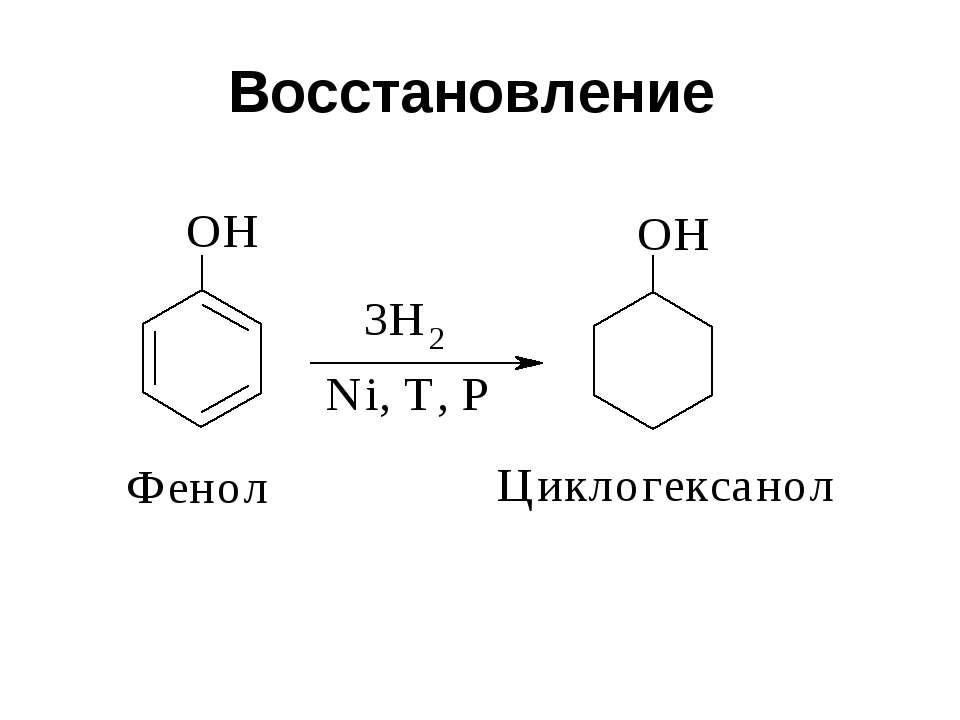
Текст слайда: Восстановление

Текст слайда: Защита функциональных групп в органическом синтезе

Текст слайда: Использование защитных групп в синтезе В многостадийном синтезе, как правило, приходится иметь дело с полифункциональными соединениями

Текст слайда: Использование защитных групп в синтезе Многие из функциональных групп должны сохраниться в неизменном виде в целевом соединении Цель защиты функциональных групп в синтезе – предотвращение их превращений в условиях проведения реакций

Текст слайда: Использование защитных групп в синтезе При этом возникают проблемы: 1) Не все функциональные группы совместимы в одной молекуле (нельзя получить магний- или литийорганическое соединение, содержащее в молекуле карбонильную функцию и т.д.)
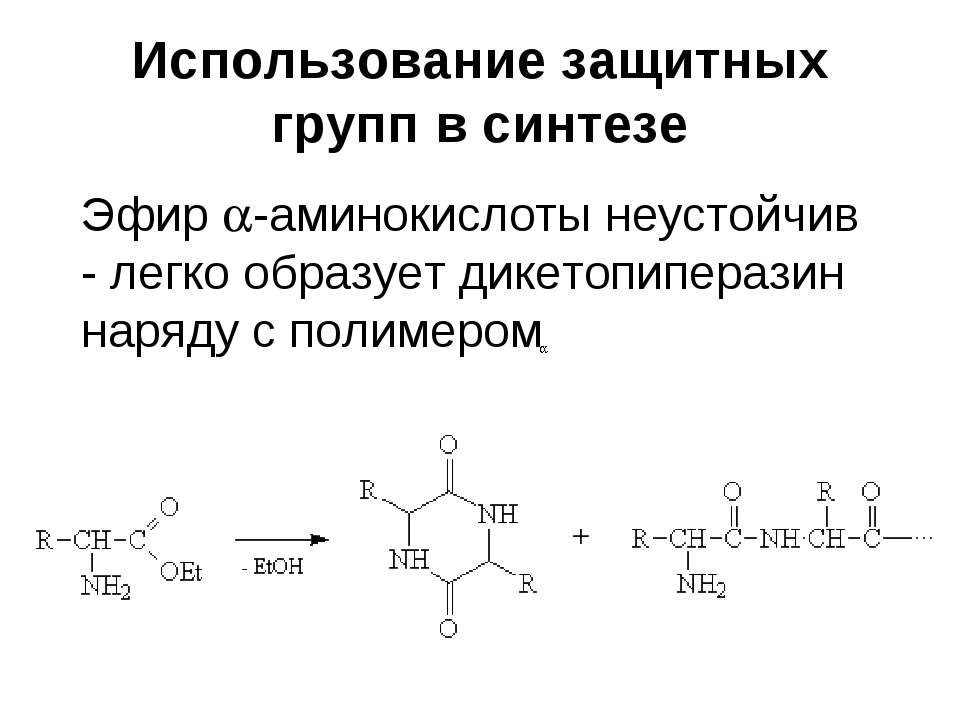
Текст слайда: Использование защитных групп в синтезе Эфир -аминокислоты неустойчив - легко образует дикетопиперазин наряду с полимером
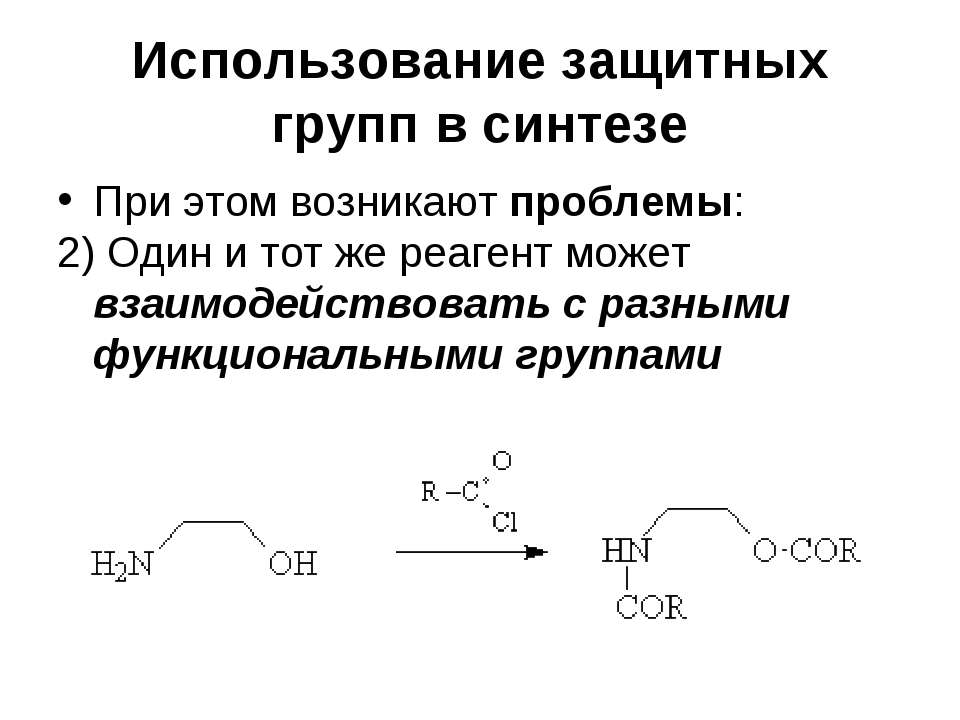
Текст слайда: Использование защитных групп в синтезе При этом возникают проблемы: 2) Один и тот же реагент может взаимодействовать с разными функциональными группами

Текст слайда: Использование защитных групп в синтезе В рассмотренных ситуациях используют избирательную блокаду тех или иных функциональных групп, создавая так называемые защитные группы, маскирующие данную функцию

Текст слайда: Использование защитных групп в синтезе Реакция Кневенагеля между ванилином и малоновой кислотой осложняется другими реакциями, связанными с наличием фенольной ОН-группы С6Н5СНО + СН2(СООС2Н5)2 С6Н5СН=С(СООС2Н5)2 + Н2О
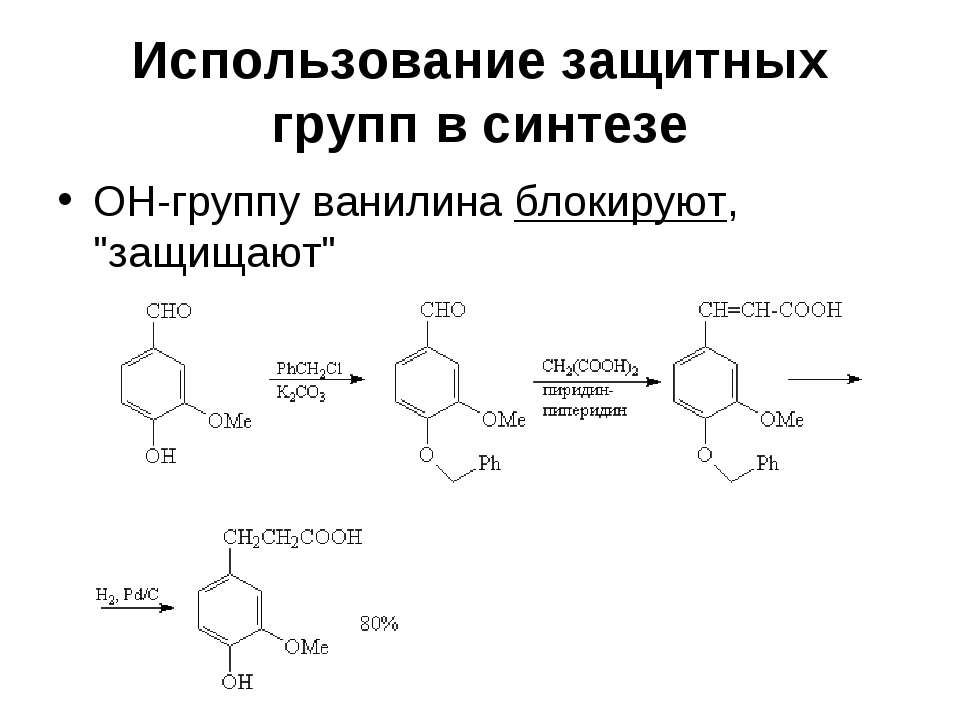
Текст слайда: Использование защитных групп в синтезе ОН-группу ванилина блокируют, "защищают"

Текст слайда: Использование защитных групп в синтезе Задача использования защитных групп включает два момента: создание защитной группы и удаление, после проведения необходимых изменений в молекуле Одну и ту же функциональную группу можно защитить различными способами
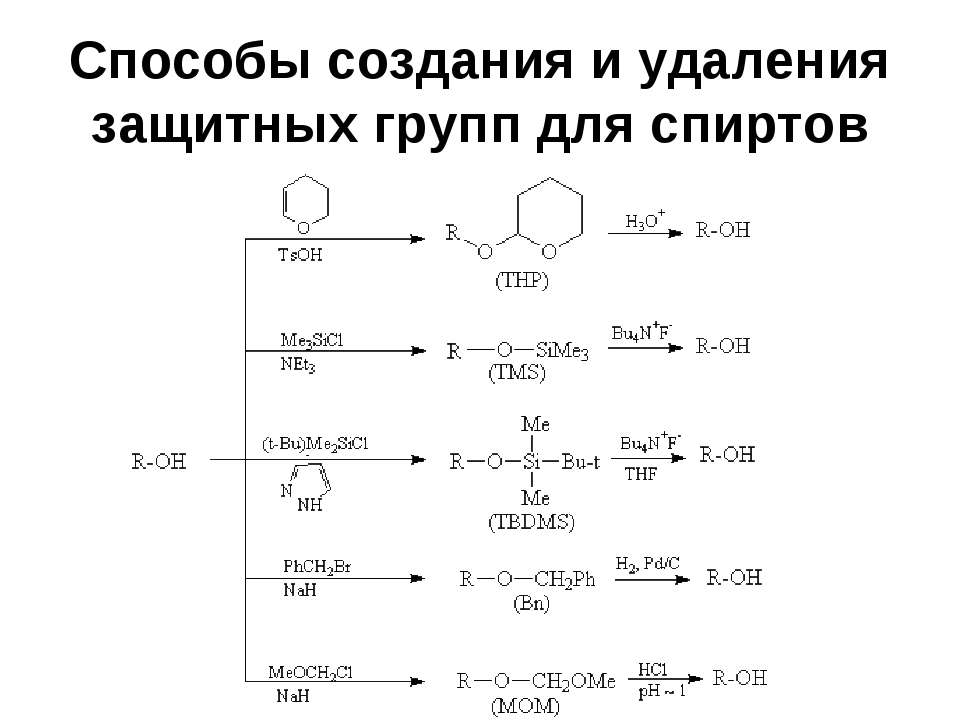
Текст слайда: Способы создания и удаления защитных групп для спиртов

Текст слайда: Использование защитных групп в синтезе Конкретную защитную группу выбирают с учетом реагентов и условий реакции так, чтобы в этих условиях защитная группа не разрушалась

Текст слайда: Использование защитных групп в синтезе Группа ТНР устойчива в щелочных условиях (рН 6-12), но неустойчива к водным растворам кислот и к кислотам Льюиса ТНР группа относительно устойчива к действию нуклеофилов и металлоорганических соединений, к гидридам, гидрированию и действию окислителей
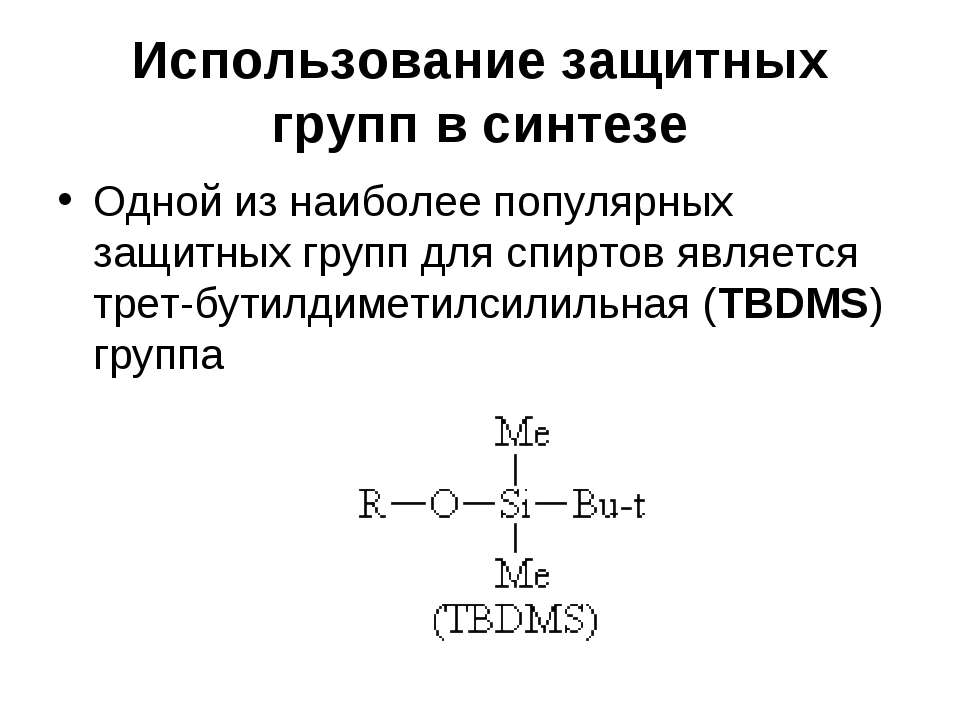
Текст слайда: Использование защитных групп в синтезе Одной из наиболее популярных защитных групп для спиртов является трет-бутилдиметилсилильная (TBDMS) группа

Текст слайда: Использование защитных групп в синтезе Эфиры спиртов с этой группой устойчивы к действию многих реагентов, причем защитная группа легко удаляется в условиях, не затрагивающих другие функциональные группы TBDMS защита приблизительно в 104 раз более устойчива к гидролизу, чем триметилсилильная (TMS) защита

Текст слайда: Использование защитных групп в синтезе Сейчас выработаны определенные стратегии, позволяющие использовать защиту различных групп в процессе данного синтеза Защитные группы в органической химии, ред. Дж.МакОми, М., Мир, 1976 P.G.M.Wuts, T.W.Green, Protective Groups in Organic Synthesis, 3nd ed., Wiley, N.-Y., 1999

Текст слайда: Использование защитных групп в синтезе В настоящее время выделяют две основные стратегические линии при использовании защитных групп: а) принцип «ортогональной стабильности» б) принцип "модулированной лабильности"

Текст слайда: Использование защитных групп в синтезе Эти принципы относятся к тем случаям, когда в процессе синтеза одновременно используются несколько различных защитных групп

Текст слайда: Принцип ортогональной стабильности Требует, чтобы каждая из используемых защитных групп удалялась в таких условиях, в которых остальные защитные группы остаются без изменений (в качестве примера можно привести сочетание тетрагидропиранильной, бензоильной и бензильной групп)
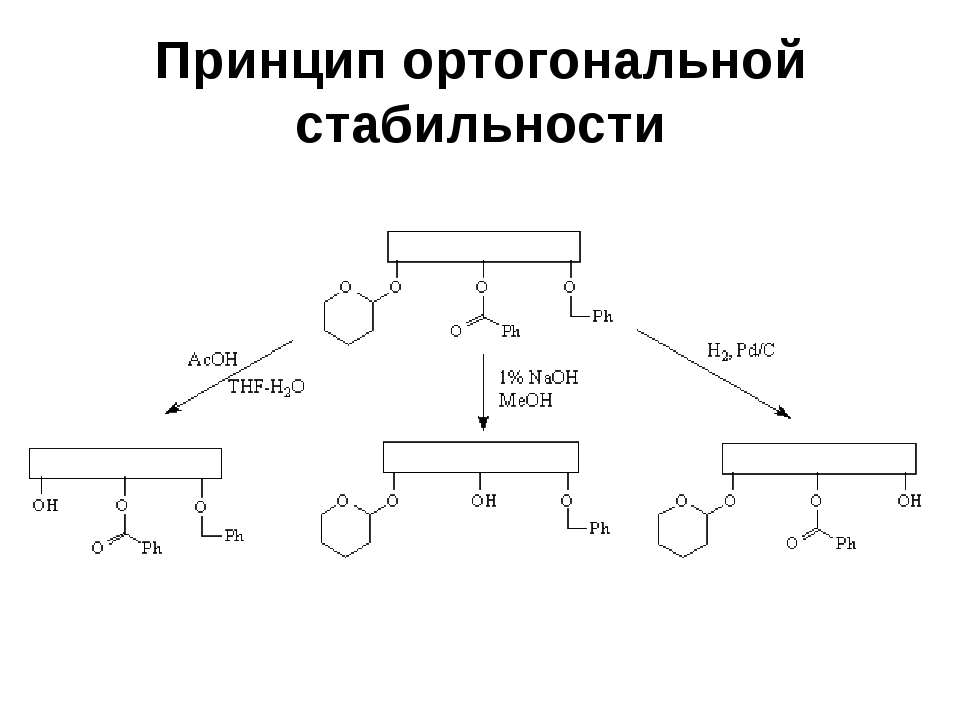
Текст слайда: Принцип ортогональной стабильности

Текст слайда: Принцип ортогональной стабильности При таком подходе данную защитную группу можно удалить на любой стадии синтеза
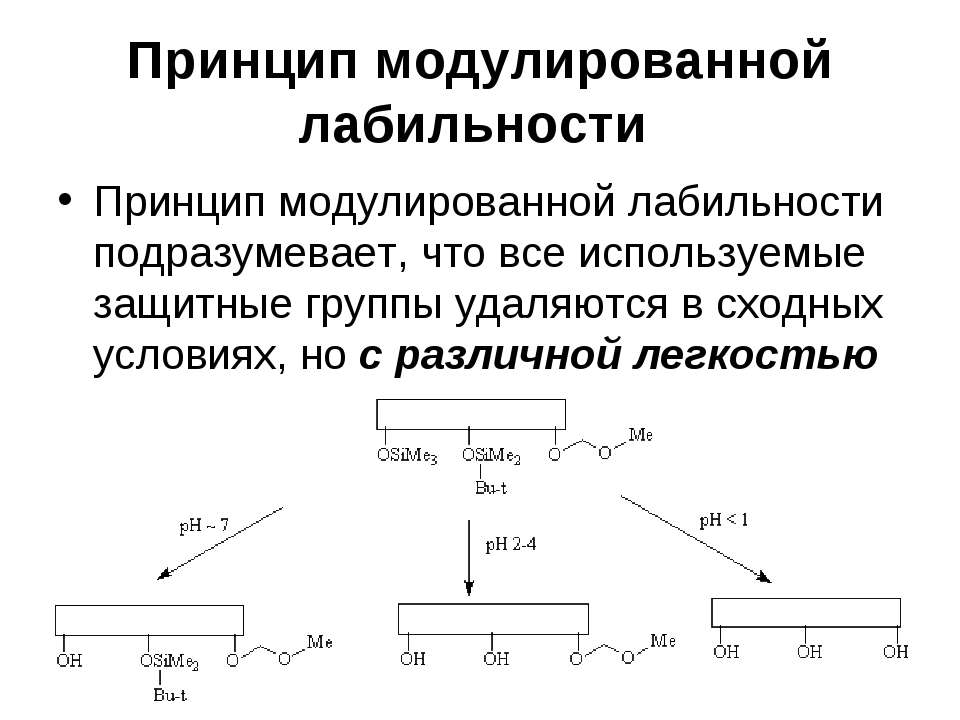
Текст слайда: Принцип модулированной лабильности Принцип модулированной лабильности подразумевает, что все используемые защитные группы удаляются в сходных условиях, но с различной легкостью

Текст слайда: Принцип модулированной лабильности При этом наименее кислотно-чувствительную метоксиметильную защитную группу нельзя удалить, не затронув остальные защитные группы

Текст слайда: Использование защитных групп в синтезе В настоящее время в арсенале химика-синтетика имеется большое число различных защитных групп Однако, синтез надо стремиться планировать так, чтобы обойтись либо совсем без защитных групп, либо свести их применение к минимуму

Текст слайда: Использование защитных групп в синтезе "The best protecting group is no protecting group" ("Самая лучшая защитная группа - отсутствие защитной группы")

Текст слайда: Использование защитных групп в синтезе Использование защитных групп в синтезе требует дополнительных операций (удлиняет и удорожает синтез) Применение защитных групп, как правило, отрицательно сказывается на выходе целевого продукта

Текст слайда: Защитные группы (некоторые примеры)
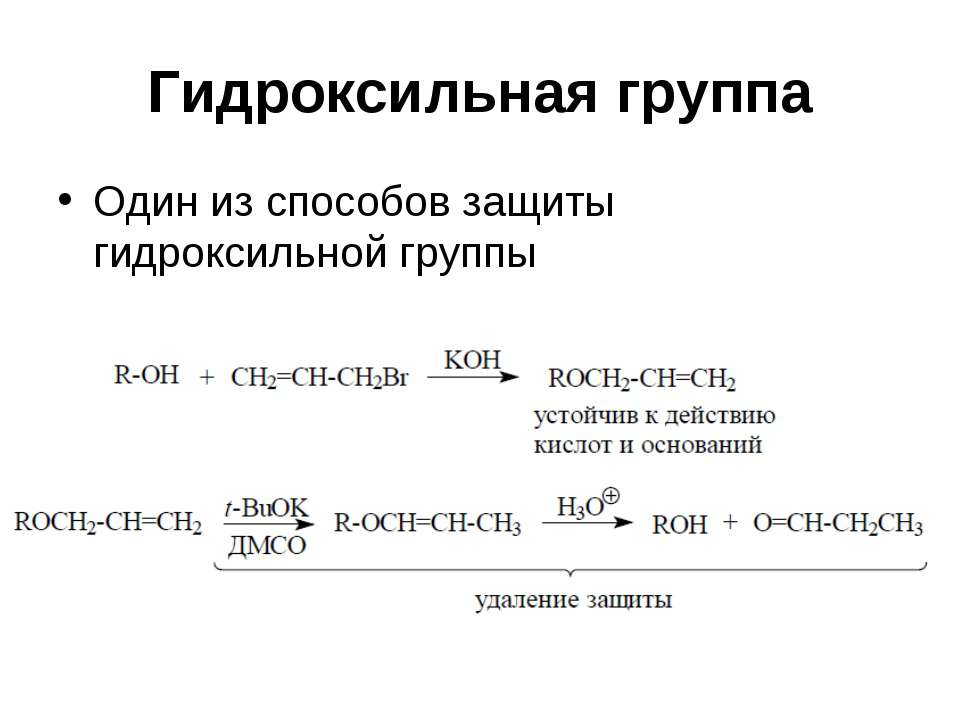
Текст слайда: Гидроксильная группа Один из способов защиты гидроксильной группы

Текст слайда: Гидроксильная группа Способ защиты Образование сложных эфиров RCOOR’ Действуют R’COCl и пиридин Защита устойчива к электрофилам, окислению Удаление защитной группы NH3 и MeOH

Текст слайда: Амины RNH2 Амиды RNHCOR’, Уретаны RNHCOOR’, Фталимиды Действуют R’COCl, Хлорформиаты R’OC(O)Cl, Фталевый ангидрид Защита устойчива к электрофилам Удаление защитной группы HO--H2O или H+-H2O, для R’= CH2Ph: H2(кат.) или HBr, для R’= t-Bu: H+, NH2NH2
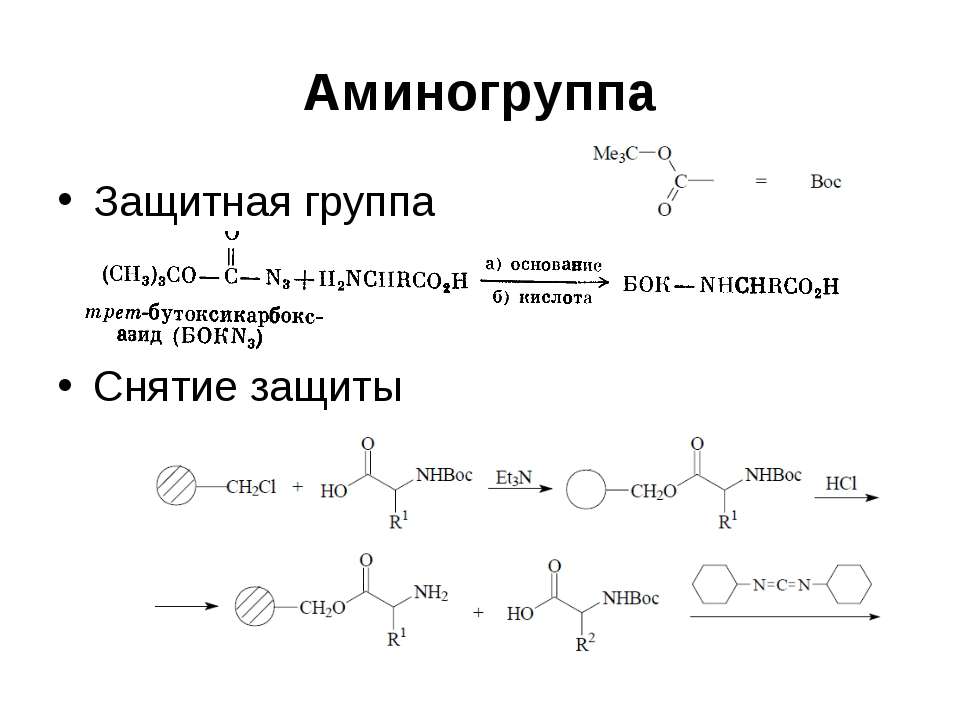
Текст слайда: Аминогруппа Защитная группа Снятие защиты
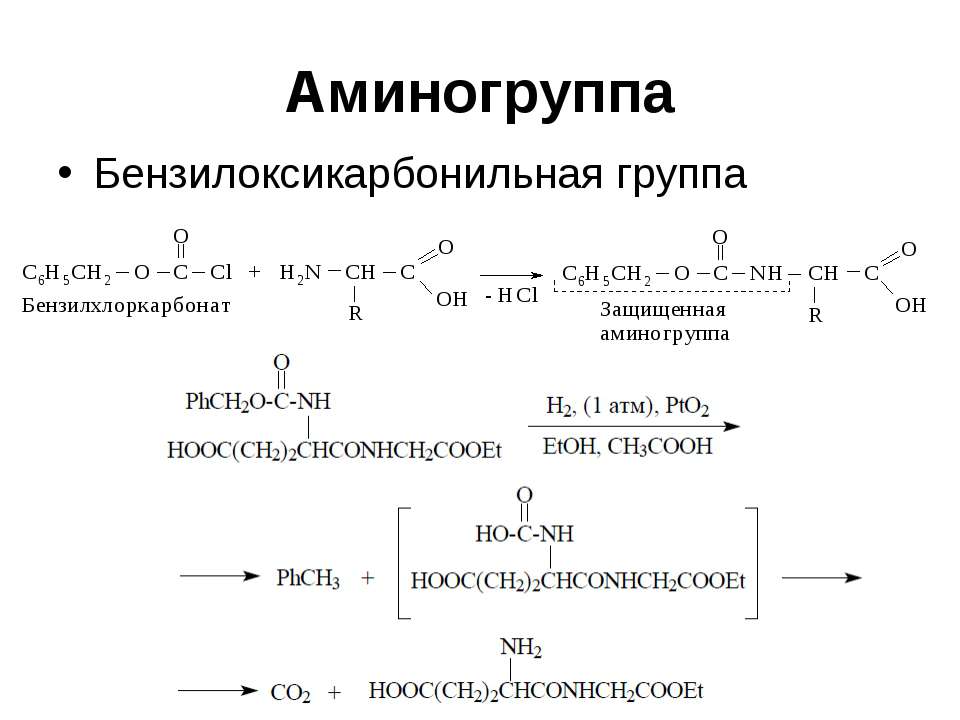
Текст слайда: Аминогруппа Бензилоксикарбонильная группа
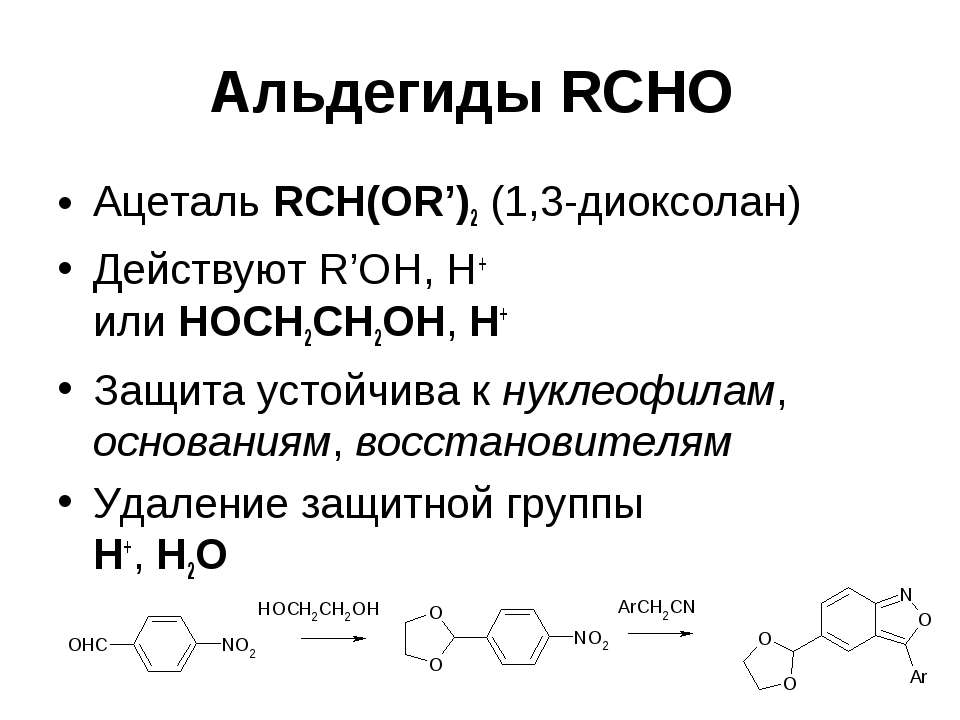
Текст слайда: Альдегиды RCHO Ацеталь RCH(OR’)2 (1,3-диоксолан) Действуют R’OH, H+ или HOCH2CH2OH, H+ Защита устойчива к нуклеофилам, основаниям, восстановителям Удаление защитной группы H+, H2O

Текст слайда: Кетоны R2CO Кеталь R2C(OR’)2 1,3-диоксолан Действуют R’OH, H+ или HOCH2CH2OH, H+ Защита устойчива к нуклеофилам, основаниям, восстановителям Удаление защитной группы H+, H2O

Текст слайда: Кислоты RCOOH Сложные эфиры: RCOOMe, RCOOEt RCOOCH2Ph, RCOOBu-t, RCOOCH2CCl3 Действуют CH2N2, EtOH и H+ PhCH2OH и H+ H+ и t-BuOH, СCl3CH2OH Защита устойчива к слабым основаниям, электрофилам Удаление защитной группы HO- и H2O, H2(кат.) или HBr, H+, Zn и MeOH

Текст слайда: Фенолы ArOH Простые метиловые эфиры или метоксиметиловые эфиры Действуют Me2SO4 и K2CO3, MeOCH2Cl и основание Защита устойчива к основаниям и слабым электрофилам Удаление защитной группы HI и HBr или BBr3, CH3COOH-H2O

Текст слайда: Тиолы RSH Защитная группа AcSR Действуют RSH+AcCl+основание Защита устойчива к электрофилам Удаление защитной группы HO--H2O
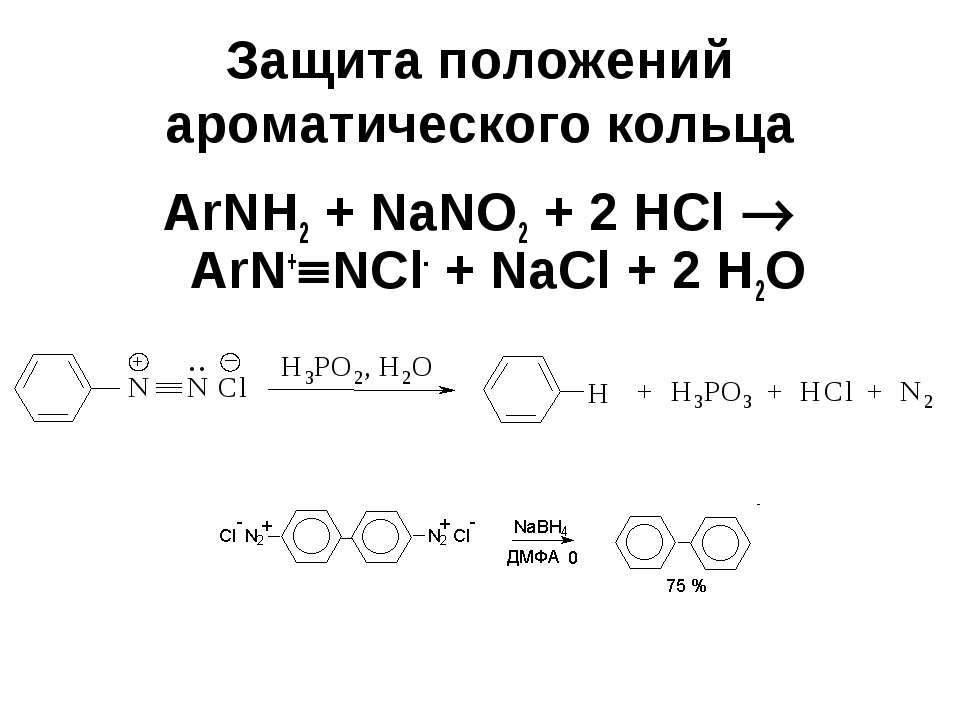
Текст слайда: Защита положений ароматического кольца ArNH2 + NaNO2 + 2 HCl ArN+ NCl- + NaCl + 2 H2O
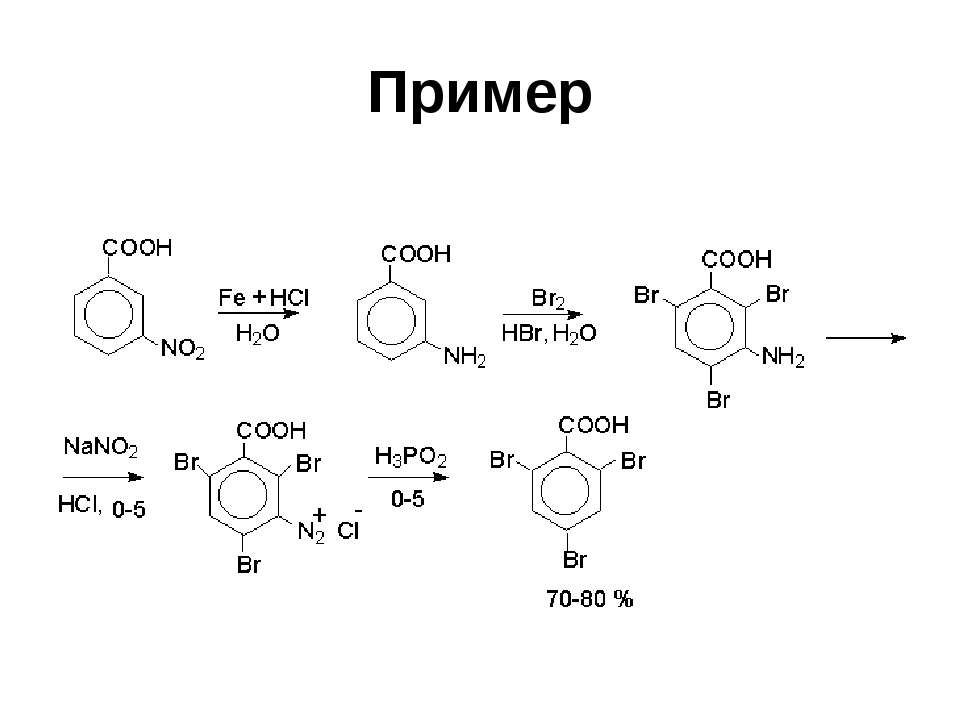
Текст слайда: Пример

Текст слайда: